2020年5月14日的《新英格兰医学杂志》上报道了美国MGH科学家 Kwang-Soo Kim团队进行的一例帕金森氏症的细胞治疗临床研究结果。这是全球第一例自体iPSC分化得到的多巴胺能神经前体细胞移植到帕金森症患者脑内的阶段性临床结果。除了之前已有报道异体的iPSC(日本Takahashi)、ESC(中国周琪院士团队)分化多巴胺前体细胞移植治疗帕金森的临床研究,这项自体移植研究具有很多借鉴意义,但同时也有许多值得探讨的地方。
首先
该研究团队通过移植多巴胺能神经前体细胞到患者自己的单核细胞制作的人源免疫小鼠模型纹状体脑区(如示意图一所示)和后续检测,证明了自体iPSC分化的细胞并不会引起免疫原性反应,但异体的H9分化的细胞会引起移植脑区的T细胞浸润,并几乎没有细胞存活。
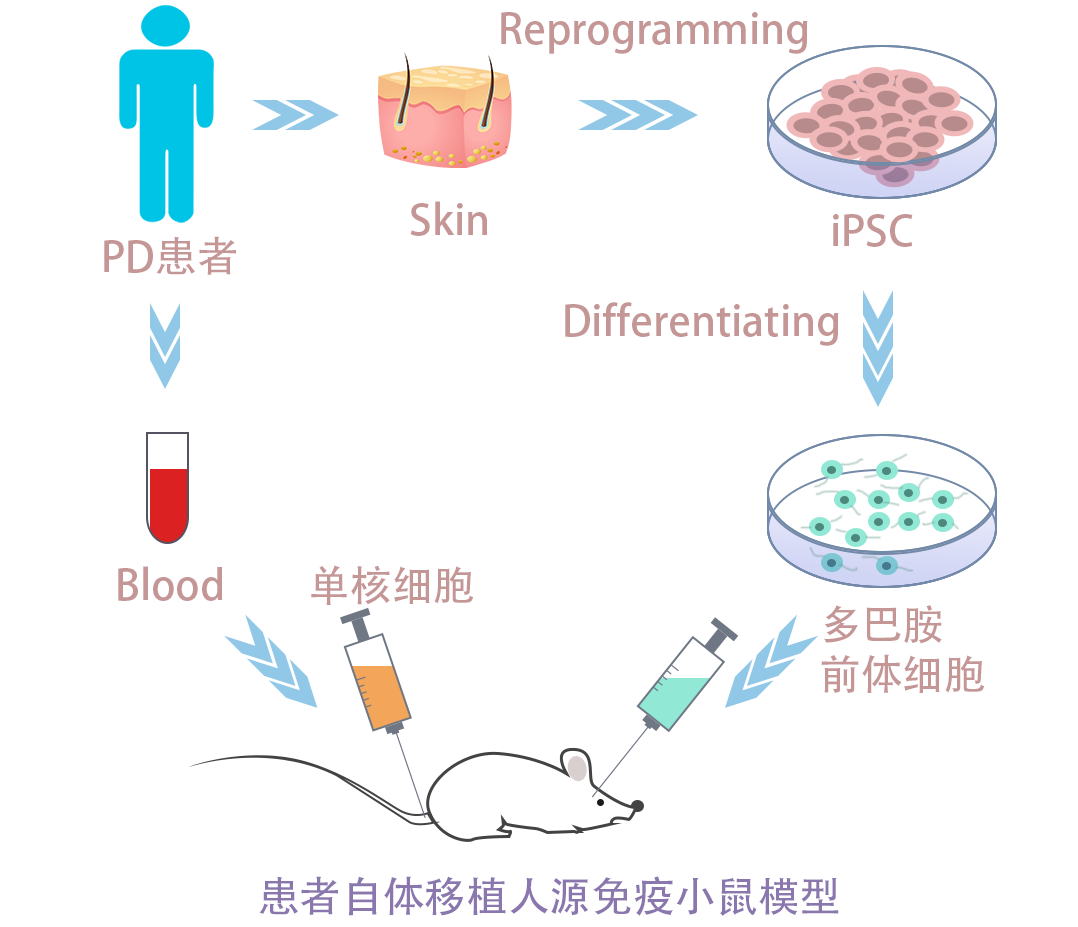
示意图一
这一结果一方面驳斥了界内iPSC分化细胞自体移植也会有免疫原性的说法,另一方面却与传统认为的大脑组织(由于血脑屏障的存在)与眼部、胎盘等均是免疫豁免的组织相冲突。
当然,已知老年人群(绝大部分帕金森患者属于的群体),大脑中风或损伤后一段时间内大脑的血脑屏障都会有更高的通透性,也有不少观察到T细胞浸润的报道。如文章自述,目前自体iPSC治疗产品由于生产及质控等成本过于高昂的原因,距离大量的临床应用仍然十分遥远。而英国ReNeuron公司及美国Neuralstem公司所完成的FDA I、II期试验使用了异体细胞颅内移植治疗脑梗塞,均只对患者进行了一个月的免疫抑制,但是在1-2年的长期跟踪下,通过影像学发现移植细胞仍然在移植区域长期存活。
因此,有可能通过在手术前后给予一定免疫抑制,能帮助避免手术等过程可能引发的血脑屏障通透,以及让移植细胞有足够时间存活和形成一定免疫识别和耐受(microglia也应在其中扮演了一定的角色),从而使通用型细胞替代疗法在神经疾病上可以得到应用。
其次
文章后面部分主要讲述,在没有使用免疫抑制剂的情况下,病人在左侧脑部进行细胞移植24个月及右侧脑部进行细胞移植18个月后,目前未观察到任何免疫排斥反应或副作用,并且其On和Off time的主要的帕金森运动功能评分均有所改善,病人自我感觉的生活质量改善评分有极大改善(见图二)。
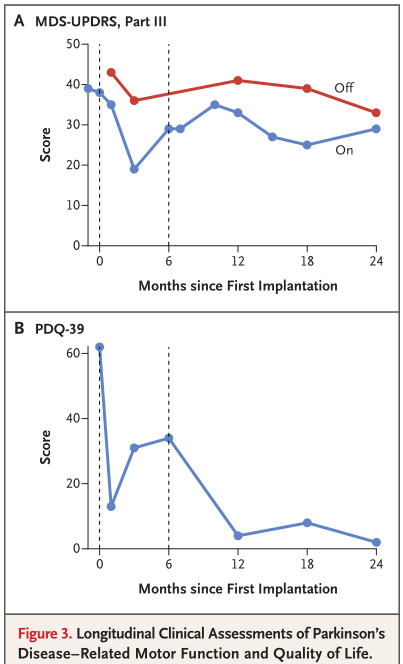
图二 来源于文献《iPSC-Derived DopamineProgenitor Cells for Parkinson’s Disease》
值得一提的是,虽然此研究使用的多巴胺前体细胞按照GMP生产,披露了各种审批和伦理的合规性,本次临床实验也通过了FDA的17145审批(可以认为相当于中国卫健委备案的、研究者发起的单人的临床研究),但正如作者在文中提到的,具有以下的主要遗憾:
1. 此次手术仅有一个患者,无法统计,并且是自我治疗意愿和自我暗示能力可能都很强的患者,无法排除评分的改善中的安慰剂效应的贡献。
2. 没有对照组和双盲,同上,无法排除安慰剂效应,也即研究只能提供一定的安全性(包括无成瘤性)的参考。
3. 患者在细胞移植治疗的同时一直服用治疗帕金森的药物(仅减少了6%的levodopa剂量,作者自己也认为不一定有显著差异),无法确认移植的细胞对此个例是否有真正的疗效。
其实同期全球有多家机构开展了多能干细胞分化的多巴胺能前体细胞移植治疗帕金森症的临床研究,包括日本京都大学的高桥淳团队及我国中科院周琪院士团队。其中高桥淳团队是最早公布采用iPSC分化细胞治疗帕金森症的临床试验,周琪院士团队则采用的是胚胎干细胞分化的多巴能神经前体细胞。已经完成CMC及临床前动物研究的Malin Parmar (瑞典 Lund University)及Lorenz Studer (美国 BlueRock Therapeutics公司)等团队也即将进行IND申报和等待获准进入临床试验。即使受试人数尚少,目前国际上开展的正规临床研究均展示了多能干细胞分化细胞用于移植治疗的2年及以上安全性及一定的有效性,使得监管部门也逐渐意识到这些新型疗法的先进性。
因此,我们将拭目以盼其他设计更加合理和规范的临床试验来继续证明多能干细胞分化的功能细胞,无论自体或异体移植治疗的长期有效性及安全性。
相关文章:
Schweitzer JS, Song B, Herrington TM, et al. Personalized iPSC-Derived Dopamine Progenitor Cells for Parkinson's Disease. N Engl J Med. 2020;382(20):1926‐1932. doi:10.1056/NEJMoa1915872
